Учёные Педиатрического университета объяснили молекулярные механизмы развития коронавирусной инфекции
Учёные Педиатрического университета объяснили молекулярные механизмы развития коронавирусной инфекции
Группа исследователей доказала, что мишенью патогенного воздействия является эндотелий (внутренняя оболочка) микрососудов. Обнаружив вирус, иммунная система стремится его уничтожить и запускает процесс апоптоза - саморазрушения клеток. Гибель эндотелиальных клеток приводит к нарушению микроциркуляции крови. Клетки органов и тканей перестают получать кислород и питательные вещества и тоже погибают. Дальнейшее развитие патологического процесса может приводить к синдрому диссеминированного внутрисосудистого свертывания (ДВС) и смерти пациента.
Статья «COVID-19 у детей: молекулярный профиль и патологические особенности» вышла в швейцарском журнале первого квартиля International Journal of Molecular Sciences. По версии журнала, опубликованная статья возглавила список последних достижений в области молекулярных исследований COVID-19. Данные учёных Педиатрического университета важны как для понимания патогенеза коронавирусной инфекции и других заболеваний, так и для поиска новых методов терапии.
|
- Это первое в мире исследование ковида у детей такого уровня. Удалось проследить патогенетические звенья, молекулярный путь, начиная от проникновения вируса. Мы выявили клетки-мишени, молекулярный механизм, лежащий в основе поражения этих клеток, последствия поражения, - сообщил один из авторов статьи, проректор по научной работе Педиатрического университета Руслан Насыров. |
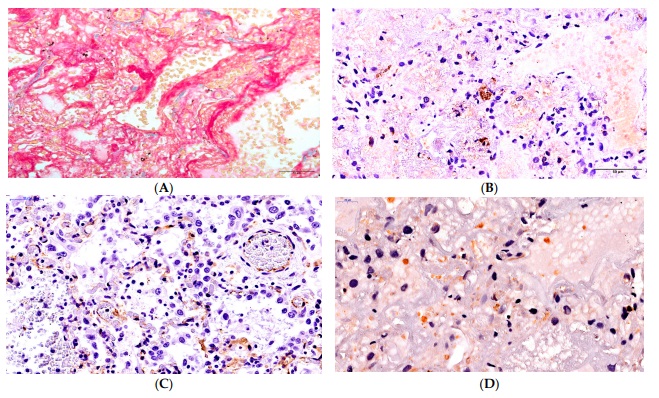
Он пояснил, что сотрудники кафедры патологической анатомии университета с начала пандемии изучали изменения тканей лёгких пациентов с разной продолжительностью заболевания, выполняли иммуногистохимические и ПЦР-исследования образцов.
|
- Иммуногистохимическая окраска показала, что нуклеокапсид (геном вируса, заключённый в белковую оболочку, прим. ред.) локализуется на стенках микрососудов. Мы обнаружили, что идёт достаточно грубое, тяжёлое поражение эндотелиальных клеток. И дальше встал вопрос: «Какой молекулярный путь к этому приводит?», - рассказал Руслан Насыров о ходе исследования. |
Выяснилось, что ключевую роль тут играет апоптоз - механизм «самоликвидации» клеток. Он постоянно имеет место и в норме: регулярная, генетически запрограммированная гибель отдельных клеток необходима для функционирования организма. Однако иногда это явление приобретает патологические формы.
|
|
- Исследуя белок апоптоза - CD-95 - мы выявили его экспрессию. Маркеры апоптоза говорят о том, что в клетках эндотелия был запущен механизм самоуничтожения, - пояснил проректор по научной работе. |
При апоптозе размер клетки уменьшается, мембрана уплотняется, образуются вздутия, завершающиеся формированием клеточных фрагментов, содержащие обломки ядер (апоптические тельца). Именно такую картину разрушения клеток эндотелия микрососудов наблюдали исследователи.
|
- Вирус, попадая в клетку, не разрушает её, он не обладает цитопатическим эффектом. Вирус наоборот «заинтересован» в сохранении клетки, поскольку он в ней размножается. Но организм, когда вирус попадает в клетку, отправляет цитокины - факторы клеточного иммунитета. Для цитокина вирус внутри клетки недосягаем, и он запускает процесс апоптоза, - рассказал Руслан Насыров. |
Термин «цитокиновый шторм», получивший широкую известность в разгар пандемии, имеет прямое отношение к этому явлению. В ряде случаев возникает необузданная реакция организма, когда огромная масса цитокинов выбрасывается в кровь и вызывает массированное нарушение гемодинамики, нередко приводящее к смерти.
Какой именно из множества известных цитокинов «нажимает на спусковой крючок» уничтожения клетки эндотелия пока неизвестно, это тема отдельного исследования. Но уже ясно, что открытия в этой области могут помочь в создании новых препаратов, эффективных против COVID-19 .
Данным же исследованием учёные Педиатрического университета доказали гипотезу о том, что эндотелий микрососудов — это первичная и доминирующая мишень воздействия патогенов.
|
- Мы доказали, что в первую очередь поражается эндотелий сосудов, а уже вторично страдают другие клетки, поскольку прекращается транспорт кислорода к ним. Это новое слово в понимании теории патологии. Из этого следует, что в случае заболевания нужно обратить особое внимание на состояние микрососудов, использовать возможные средства для защиты сосудов, - резюмировал Руслан Насыров. |
Представленные результаты имеют важное значение для разработки методов исследования эндотелия, создания и использования новых эндотелийпротекторных препаратов при COVID-19, а также профилактики других заболеваний, в том числе неинфекционного происхождения.
Читать статью «COVID-19 у детей: молекулярный профиль
и патологические особенности» >>>